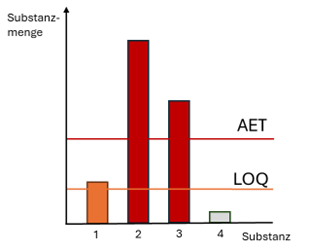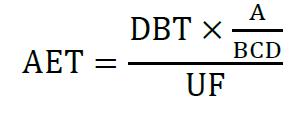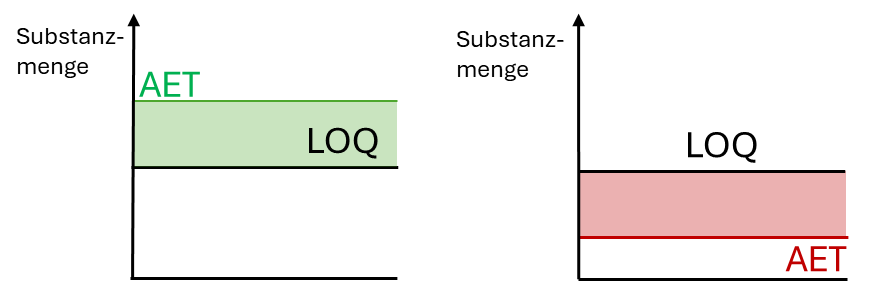Biokompatibilität: Risiken falscher AET-Festlegungen bei chemischer Charakterisierung und toxikologischer Risikobewertung
Die chemische Charakterisierung nach DIN EN ISO 10993-18:2023-11 und die toxikologische Risikobewertung (TRA) nach DIN EN ISO 10993-17:2024-02 sind wesentliche Bestandteile der biologischen Beurteilung von Medizinprodukten. Ein kritischer Parameter in diesem Prozess ist die analytische Beurteilungsschwelle (AET; eng. Analytical Evaluation Threshold).
Die korrekte Festlegung des AET ist entscheidend, um sicherzustellen, dass alle relevanten Extractables & Leachables bewertet werden. In diesem Artikel werden die potenziellen Konsequenzen einer fehlerhaften Festlegung der relevanten Variablen zur Berechnung des AET beleuchtet.
Bedeutung des AET
Der AET (siehe Abb. 1) dient als Schwellenwert, unterhalb dessen chemische Verbindungen als toxikologisch unbedenklich betrachtet werden. Daher reicht eine Auswertung bis zum AET in den meisten Fällen aus. Werden besonders besorgniserregenden Stoffe (SVHC; eng.Substance of Very High Concern) oder CoC (Cohorts of Concern) erwartet, müssen diese gesondert betrachtet werden.
Um den AET als Bewertungsgrenze nutzen zu können, ist es wichtig, dass er auch technisch umsetzbar ist. Jedes Labor hat seine eigenen, intern definierten Quantifizierungsgrenzen (LOQ; eng. Limit of Quantification), die unterhalb des definierten AET liegen müssen.
In Abb. 1 wird die Relation zwischen dem AET und LOQ im Optimalfall dargestellt. Substanzen 2 und 3 (rot) liegen oberhalb des AET und müssen daher ausgewertet und toxikologisch betrachtet werden. Substanz 1 (orange) und 4 (grau) müssen hingegen nicht betrachtet werden. Handelt es sich in diesem Fall um CoC oder SVHC, wäre eine Auswertung lediglich für Substanz 1 möglich, da sich Substanz 4 unterhalb des LOQs befindet und daher nicht quantifiziert werden kann. Durch diverse Beschränkungen und Ausnahmen sollte diese Herangehensweise durch einen Toxikologen verifiziert werden.
Berechnung des AET
Die Berechnung des AET erfolgt gemäß DIN EN ISO 10993-18:2023-11 wie in der Formel (Abb. 2). dargestellt. Im Folgenden wird auf die Bedeutung der einzelnen Kenngrößen in der AET-Gleichung eingegangen.
DBT - dosisbasierter Schwellenwert
Häufig wird für den DBT der TTC (Threshold of Toxicological Concern) herangezogen. Dieser ist abhängig von der Anwendungsdauer des Medizinproduktes (ISO/TS21726). Je länger die Anwendungsdauer ist, desto niedriger fällt dieser Wert aus. Auch hier kann eine nachträgliche Anpassung (Verringerung) dazu führen, dass der AET unter den LOQ fällt.
A – Anzahl der extrahierten Medizinprodukte
B – Extraktionsvolumen
Die DIN EN ISO 10993-12 gibt Empfehlungen, welches Extraktionsverhältnis für ein Medizinprodukt verwendet werden sollte. Die berechneten Volumina beziehen sich entweder auf die Oberfläche oder das Gewicht des Medizinproduktes. Bei bestimmten Geometrien ist es notwendig, dass das Volumen erhöht wird, um den gesamten Prüfkörper bedecken zu können.
Bei einem sehr kleinen DBT oder bei sehr hohen Volumina (B), z.B. durch sehr große Prüfkörper oder durch Erhöhung des Volumens aufgrund der Geometrie, ist es möglich, dass der AET den LOQ unterschreitet.
C – Anzahl der üblicherweise pro Patienten gleichzeitig angewendeten Medizinprodukte
Dieser Wert sollte auf Grundlage der tatsächlichen Anwendung festgelegt werden. Nachfolgend verschiedene Beispiele:
Wundhaken:
Es werden 2 Wundhaken benötigt, um eine Wunde aufzuhalten (C=2).
Dentalimplantate:
Üblicherweise werden nicht mehr als 2 Zähne durch Implantate ausgetauscht. (C=2).
Als Worst-Case können maximal 4 Zähne durch Implantate ausgetauscht werden (C=4).
Werden diese z.B. nach 10 Jahren erneut ausgetauscht, beträgt der C-Wert weiterhin 4.Katheter:
Der Katheter wird jeden Tag gewechselt, aber es wird nur ein Katheter gleichzeitig angewendet (C=1).
Wird der C-Wert nach der Durchführung der Analysen korrigiert (erhöht) kann der AET unter den LOQ fallen.
D - Konzentrations- oder Verdünnungsfaktor
Faktor zur Berücksichtigung der während der Analyse durchgeführten Konzentration (D<1) und Verdünnungsschritte (D>1).
UF – Unsicherheitsfaktor
Durch die Auswertung mittels Semiquantifizierung (Berechnung der Menge anhand repräsentativer Standards anstelle einer exakten Quantifizierung) kann es zu Abweichungen vom tatsächlichen Wert kommen. Dies ist darauf zurückzuführen, dass jede Substanz einen anderen Ansprechfaktor aufweist. Das bedeutet, dass das Integral des Peaks im Chromatogramm nicht nur durch die Menge, sondern auch durch Wechselwirkungen mit der Chromatographie-Säule o.ä. beeinflusst wird. Mit Hilfe der UF ist es möglich, diese Schwankungen zu berücksichtigen. Dieser Wert ist durch das Analyseverfahren festgelegt und kann nicht beeinflusst werden.
Problematik
Die Berechnung des AET kann zwei unterschiedliche Szenarien aufzeigen (vgl. Abb. 3). Liegt der AET oberhalb des LOQ, so ist die Methode empfindlich genug, um toxikologisch relevante Substanzen zu quantifizieren (grün). Liegt der AET hingegen unterhalb des LOQ, so entsteht eine Lücke (rot), in der die Substanzen mit der Methode nicht ausreichend genau quantifiziert werden können.
Szenario 1: AET fällt durch Anpassung unter LOQ
Wird der AET vor Beginn der chemischen Charakterisierung zu hoch festgelegt und muss dieser im Rahmen der toxikologischen Risikobewertung später erhöht werden, so kann es zu dem Ergebnis kommen, dass die Extrakte nicht ausreichend hoch aufkonzentriert wurden. In direkter Konsequenz kann nicht ausgeschlossen werden, dass toxikologisch relevante Verbindungen nachgewiesen und quantifiziert werden konnten. Dies wirkt sich negativ bei der toxikologischen Risikobewertung aus.
Szenario 2: AET steigt durch Anpassung
Wird der AET vor Beginn der chemischen Charakterisierung zu niedrig festgelegt, so ist eine nachträgliche Erhöhung im Rahmen der toxikologischen Risikobewertung möglich. Die Konsequenzen sind weniger problematisch als im Falle eines zu niedrigen AET.
Vorbeugende Maßnahmen - Gegenmaßnahmen
Sofern im Voraus ersichtlich ist, dass der AET den LOQ unterschreiten wird, besteht die Möglichkeit, im Vorhinein verschiedene Gegenmaßnahmen zu ergreifen. Mögliche Gegenmaßnahmen sind:
- Konzentration der Extrakte (D<1)
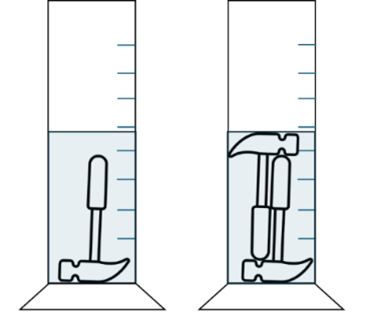
Gleichzeitige Extraktion mehrerer Prüfgegenstände (Poolung, A), um die geometriebedingte Erhöhung des Volumens zu minimieren (Abb. 4).
In Anbetracht der hohen Variabilität von Medizinprodukten ist dies jedoch stets eine Einzelfallentscheidung. Daher ist es besonders wichtig, realistische und gut durchdachte Angaben zu den einzelnen Variablen zu machen.
Fazit
Die korrekte Festlegung des AET ist entscheidend für die Richtigkeit der chemischen Charakterisierung und des toxikologischen Risikobewertungsverfahrens. Eine zu niedrige oder zu hohe Festlegung des AET kann zu erheblichen Problemen führen, welche die Bewertung der chemischen Charakterisierung im Rahmen der biologischen Beurteilung beeinträchtigen.
Daher ist es wichtig, den AET sorgfältig und präzise zu bestimmen, um eine umfassende und zuverlässige Bewertung zu gewährleisten. Das Prüflabor ist daher darauf angewiesen, dass der Hersteller sich im Vorfeld mit diesen Kriterien beschäftigt und die relevanten Variablen C (Anzahl der gleichzeitig angewendeten Medizinprodukte) und DBT (dosisbezogener Schwellenwert) direkt und korrekt mit dem Prüfauftrag angibt.
Whitepaper zum Download
Newsletter Anmeldung